





Категория: Бланки/Образцы
Стоимость заполнения: 7 000 руб./ 1 месяц заполнения
Сроки заполнения: от 1-го дня
* В стоимость входит заполнение абсолютно всех журналов, независимо от количества.
Сроки доставки по Москве и Московской области: 1 день [всегда есть на складе]
Сроки доставки по регионам РФ: 2-5 дней [всегда есть на складе]
* Быстрая доставка почтовым оператором по всем регионам РФ
* В стоимость входит консультация по работе с журналами: правильное ведение / заполнение / отчетность.
* В стоимость НЕ входят сами журналы. При Вашем желании, их можно приобрести у нас для конкретной деятельности: медицина, общепит, салоны красоты, фармацевтика, проиводство и др. Всегда в наличии в Москве и Санкт-Петербурге.
* Покажем как заполнять;
* Предложим услугу ежемесячного заполнения журналов.
Стоимость покупки 1 журнала: 290 руб. с адаптацией требованиям Роспотребнадзора (СЭС, ФБУЗ «Центра гигиены и эпидемиологии»).
* Можем использовать Ваши журналы для заполнения или предложить свои.
Ведение дезинфекционного режима в организациях подтверждается ведением журнала (книга) учета дезсредств с расчетом, регистрацией и гарантией
E-mail: This email address is being protected from spambots. You need JavaScript enabled to view it. This email address is being protected from spambots. You need JavaScript enabled to view it.
(499) 110-91-64 — Ваш личный менеджер ведения санитарной документации по РФ в Москве
(Москва, ул. Касаткина, д. 11)
(812) 407-22-64 — Ваш личный менеджер ведения санитарной документации по РФ в Санкт-Петербурге (Санкт-Петербург, Синопская наб. д. 22)
 Предлагаем следующий порядок работы:
Предлагаем следующий порядок работы:
— по договоренности наш курьер приезжает и забирает журналы
— в течение нескольких дней мы ведем заполнение
— по договоренности наш курьер приезжает и отдает журналы
* Оплата удобным для вас способом (нал./безнал). 100% предоплата.
* Сроки заполнения могут быть сокращены до 1 дня.
Заполним журналы за Вас! Ежемесячно! Журналы обязательного ведения. Продажа и заполнение
В настоящий момент у нас обслуживаются виды деятельности:
— общественное питание;
— салоны красоты;
— медицинские центры;
— стоматологии;
— гостиницы;
— образовательные учреждения;
— аптеки и аптечные пункты;
— и другие.
Ждем Вашего звонка!
Ваши вопросы / наши ответы по электронной почте
Реактивы, входящие в состав азопирама. и его растворы должны храниться в плотно закрывающихся емкостях отдельно от пищевых продуктов, лекарственных препаратов, дезинфицирующих средств, крепких кислот и щелочей.
При попадании на кожу азопирама или веществ, входящих в его состав, а также перекиси водорода, их следует удалить чистой ватой или марлей (ветошью) и обмыть место контакта водой. При попадании реактивов на слизистые после немедленного удаления вещества следует место контакта обильно промыть большим количеством холодной воды.
Рассыпанные или пролитые реактивы удаляют, а место, где они находились, промывают или протирают тампонами, смоченными водой или спиртом.
Азопирам горюч, т.к. в его состав входит спирт. Поэтому нельзя допускать контакт азопирама с открытым огнем и раскаленными поверхностями нагревательных приборов.

Качество предстерилизационной очистки на остатки моющих средств контролируют с помощью фенолфталеиновой пробы (рис.78).
Рис.78 Фенолфталеин
При положительной фенолфталеиновой пробе о наличии на изделиях следов щелочных компонентов моющего средства свидетельствует появление розового окрашивания реактива, при их отсутствии – цвет, смоченного в фенолфталеиновом растворе тампона, не меняется.
Данной пробой проверяется также качество приготовления моющего раствора, цвет фенолфталеиновой пробы должен стать малиновым, если моющий раствор приготовлен правильно.
Результаты проверки качества обработки инструментов (азопирамовой и фенолфталеиновой проб) заносятся в журнал учета качества предстерилизационной очистки.
При положительной пробе на кровь всюпартию контролируемых изделий, от которой отбиралсяконтроль, подвергают повторной обработке с самого начала до полученияотрицательных результатов.
При положительной пробе на моющее средство всюпартию контролируемых изделий, от которой отбиралсяконтроль, подвергают повторному промыванию под проточной водой и в дистиллированной до полученияотрицательных результатов.
Стерилизация
Стерилизация – это полное уничтожение всех микроорганизмов и их спор на инструментарии, перевязочном материале.
Любые предметы, применяемые при лечении и уходе за пациентами, если они не будут полностью обеззаражены, могут привести к инфицированию других людей. Использование недостаточно простерилизованного инструментария может вызвать развитие парентерального гепатита, СПИДа, стафилококковой и других инфекций.
Стерилизации подвергаются все инструменты, средней и высокой степени риска инфицирования: изделия, соприкасающиеся с раневой поверхностью, контактирующие с кровью или инъекционными препаратами и медицинские инструменты, которые в процессе эксплуатации соприкасаются со слизистой оболочкой и могут вызвать её повреждение.
Стерилизацию проводят после предстерилизационной очистки с отрицательными результатами проб на следы крови (азопирамовая) и щелочных компонентов синтетических моющих средств (фенолфталеиновая проба).
Для пациентов, перенесших вирусный гепатит, используется только шприцы и иглы однократного применения!
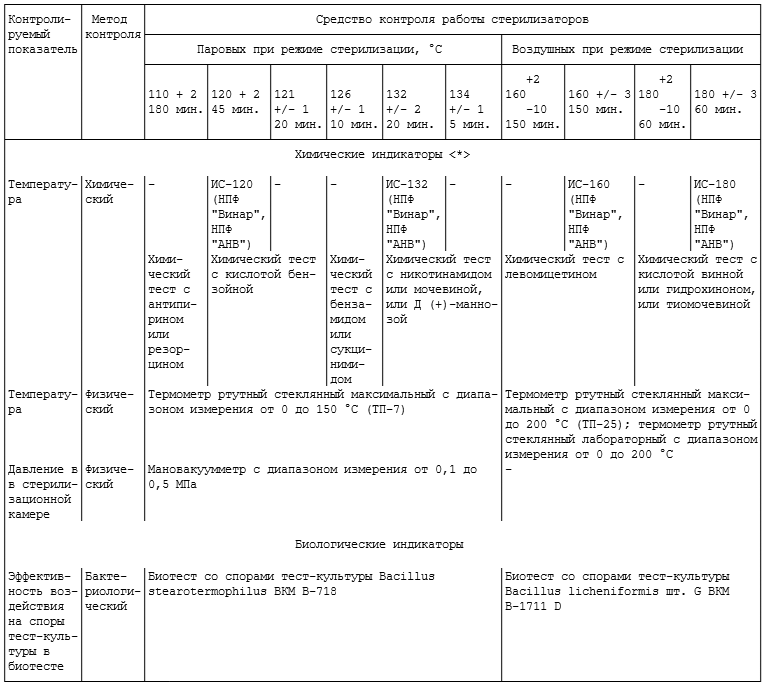
Виды, методы и режимы стерилизации (см. таблицу)
окись этилена в смеси с углекислым газом, бромистым метилом и др.
Для проведения паровой стерилизации используют паровые стерилизаторы (автоклавы) (рис.79). Стерилизующим средством является водяной насыщенный пар под избыточным давлением.
Рис.79 Паровой стерилизатор
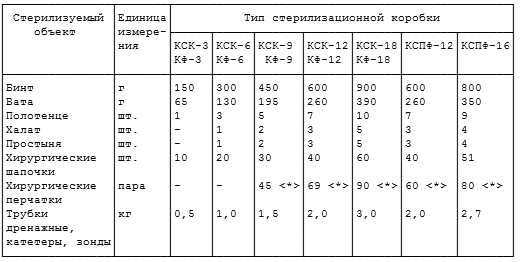
Паровым методом стерилизуют общие хирургические и специальные инструменты, детали приборов и аппаратов из коррозионностойких металлов, стекла, шприцы с пометкой 200°С, хирургическое белье, перевязочный и шовный материал, изделия из резин (перчатки, трубки, катетеры, зонды и т.д.), латекса, отдельных видов пластмасс.
Виды упаковки и сроки сохранения стерильности:
При стерилизации паровым методом материал упаковывают в стерилизационные коробки с фильтром или без фильтра (рис.80), двойную мягкую упаковку из бязи. пергамент, крафт-бумагу (рис.81), бумагу влагопрочную (рис.82), бумагу высокопрочную, бумагу крепированную (рис.83).
Срок сохранения стерильности изделий, простерилизованных в стерилизационной коробке без фильтра, в двойной мягкой упаковке. крафт-бумаге – 3 суток, в пергаменте, бумаге влагопрочной, бумаге высокопрочной, бумаге крепированной, стерилизационной коробке с фильтром – 20 суток. В современных упаковках и более 20 суток.
При открытой стерилизационной коробке любого образца стерильность материалов, изделий сохраняется до 24 часов.



Рис.80 Стерилизационные коробки с фильтром и без фильтра
Рис.81 Крафт-пакет для стерилизации


Рис.82 Пакеты влагопрочные для стерилизации
Рис.83 Крепированная бумага для стерилизации
Сроки использования изделий контролируются проставляемыми на бирках стерилизационных коробок датами, временем стерилизации, датами и временем вскрытия (первые помечаются работниками ЦСО или автоклавной, вторые выполняются медицинскими сестрами отделений).
Рис.84 Индикаторы стерильности ИС-120
Для контроля паровой стерилизации применяют термовременные ленты фирмы «Винар» – ИС-132, ИС-120 (рис.84). Это современные тесты контроля стерилизации, представляющие собой бумажные полоски с нанесенными на одну сторону специальным индикаторным составом, который меняет цвет при заданном режиме стерилизации (температуре и времени) и подтверждает наличие пара в стерилизаторе. 
Виды укладки биксов:
а) универсальная – в стерилизационную коробку укладывают материал для накрытия «стерильного стола»;
б) целевая укладка – в стерилизационную коробку укладывают белье и перевязочный материал, необходимый для определенной операции;
в) видовая укладка – в стерилизационную коробку кладут только один вид изделия (операционное белье или перевязочный материал и др.).
Правила упаковки материала в стерилизационные коробки :Простерилизованные изделия должны оставаться в автоклаве в течение 1,5 –2 часа до полного остывания. Во время остывания не должно быть сквозняков в помещении и доступа холодного воздуха. ЦСО должна быть оборудована приточно-вытяжной вентиляцией. При разгрузке стерилизатора исключается присутствие других сотрудников ЦСО, кроме персонала стерильной зоны.
После стерилизации стерилизационные коробки выдаются в отделения только остывшими в 2-х мешках, один из которых снимается перед входом в кабинет.
Воздушный метод стерилизации сухим горячим воздухом
При воздушном методе стерилизации стерилизующим средством является сухой горячий воздух, стерилизацию осуществляют в воздушных стерилизаторах (рис.85).
Рис.85 Воздушный стерилизатор
Воздушным методом стерилизуют хирургические, гинекологические, стоматологические инструменты, детали приборов и аппаратов, в том числе изготовленные из коррозионнонестойких металлов, шприцы с пометкой 200°С, инъекционные иглы, изделия из силиконовой резины. 
Сухим жаром стерилизуют некоторые термостойкие порошки, масла, тальк, стеклянную тару (ампулы, флаконы и необходимую посуду), вспомогательные материалы.
Стерилизации подвергаются сухие изделия.
1. 180°С, 60 минут
2. 160°С, 150 минут
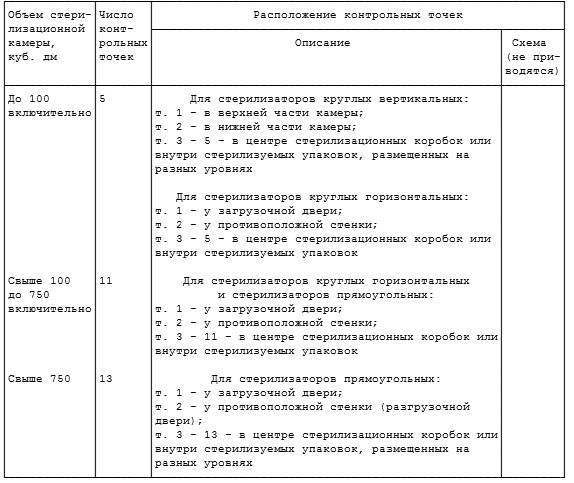
Качество стерилизации воздушным методом зависит от равномерности распределения горячего воздуха в стерилизационной камере, что достигается правильной загрузкой стерилизатора. Изделия загружают в таком количестве, которое допускает свободную подачу воздуха к стерилизуемому изделию. Изделия выкладывают на перфорированные решетки, располагая их в один слой, не соприкасаясь друг с другом, занимая до 70% площади решетки. Крупные изделия стерилизуют на верхних полках.
Стерилизаторы нельзя открывать во время процесса стерилизации, так как температура резко падает, и могут образоваться воздушные карманы с разницей температур в 30-40°С.
Виды упаковки и сроки сохранения стерильности:
Изделия, стерилизуемые в открытом виде без упаковки (рис.86), помещаются на рабочий стол и используются в течение одной рабочей смены. 
Рис.86 Стерилизация без упаковки
Если же предметы простерилизованы в крафт-бумаге. они сохраняют стерильность до трех суток.
Стерильность изделий, простерилизованных в бумаге влагопрочной, бумаге высокопрочной, бумаге крепированной. сохраняется до 20 суток.
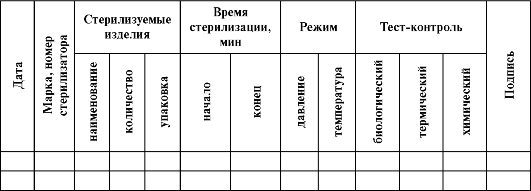
Рис.87 Журнал контроля работы стерилизаторов
Для контроля воздушной стерилизации применяют термовременные ленты фирмы «Винар» – ИС-180, ИС-160. Термотесты укладываются на каждую полку воздушного стерилизатора в виде конверта в пяти точках по четырем краям и в середине. Если хотя бы один химический тест не изменил цвет, стерилизацию всей партии инструментов проводят заново. 
Работа стерилизаторов отражается в журнале контроля работы стерилизаторов воздушного, парового (автоклава) (рис.87).
Правила укладки изделий медицинского назначения в крафт-пакет.
Одним из обязательных условий эффективной стерилизации является правильная укладка изделий перед проведением стерилизации, выбор оптимальных защитных упаковок.
Рациональная упаковка и укладка бельевых, инструментальных и других наборов способствуют полному удалению воздуха из стерилизуемого материала и проникновению стерилизующего агента в самые глубокие точки упаковок. Максимальное удаление воздуха из камеры и упаковок приводит к тому, что в любом участке стерилизуемых изделий достигается требуемая для стерилизации температура.
В один крафт-пакет укладывается один инструмент!
Стеклянные многоразовые шприцы упаковываются в разобранном состоянии, поршень вынимается из канала шприца. рядом помещаются две иглы: одна – для набора лекарственного средства, другая – для выполнения инъекции.
Размер пакетов подбирается таким образом, чтобы между материалом и краем с термошвом оставался промежуток не менее 3см. Это необходимо сделать, чтобы пакет был закрыт без образования складок, а также во избежание повреждений упаковки.
Заполнение пакетов материалом должно проводиться таким образом, чтобы материал занимал не более ? возможного объема, чтобы нижние, боковые и верхние швы не были напряжены. Перед запечатыванием пакетов из них ладонью руки необходимо выдавить воздух, чтобы избежать чрезмерно высокого давления и разрыва запечатанных швов.
Пакеты должны сохранять герметичность и сравнительно легко подвергаться утилизации.
Инфракрасный метод стерилизации
Метод основан на применении нового термического агента – кратковременного импульсного инфракрасного излучения, создающего в рабочей камере стерилизатора температуру 200+3°С. Полный цикл стерилизации стоматологических и микрохирургических инструментов в неупакованном виде занимает в инфракрасном стерилизаторе от 10 до 25 минут (в зависимости от инструментов), включая этапы выхода на режим и охлаждение, после чего инструменты могут использоваться по назначению. Конструкция этих стерилизаторов позволяет целиком размещать в стерилизационной камере и стерилизовать, и затем оставлять для охлаждения даже стоматологические щипцы.
Рис.88 Гласперленовый метод стерилизации
В стерилизаторах, стерилизующим средством в которых является среда нагретых стеклянных шариков (гласперленовые шариковые стерилизаторы), стерилизуют изделия, применяемые в стоматологии (боры зубные, головки алмазные, дрильборы, а также рабочие части гладилок, экскаваторов, зондов и др.).
Изделия стерилизуют в неупакованном виде по режимам, указанным в инструкции по эксплуатации конкретного стерилизатора, разрешённого для применения. После стерилизации инструменты используют сразу по назначению.
Радиационный метод стерилизации
Внедрение в медицинскую практику большого количества изделий из термолабильных материалов потребовало применения так называемых «холодных» методов стерилизации, одним из которых является радиационный метод. Источником ионизирующих излучений служат долгоживущие изотопы кобальта и цезия.
Радиационная стерилизация, ставшая одним из основных методов стерилизации термолабильных изделий медицинского назначения, обладает рядом технологических преимуществ. Основными достоинствами этого метода являются: высокая степень инъактивации (потеря своей активности) микроорганизмов, возможность стерилизации больших партий материалов, автоматизация процесса, стерилизация изделий в любой герметичной упаковке и товарной таре.
Радиационный метод используется для промышленной стерилизации одноразовых изделий из полимерных материалов: шприцы, инъекционные иглы, катетеры, системы для переливания крови, режущих инструментов, шовных материалов, перевязочных материалов, ряда лекарственных препаратов и т.д.
В лечебно-профилактических организациях радиационная стерилизация не применяется в связи с большой дороговизной и по соображениям техники безопасности. Однако в последние годы изучаются возможности создания оборудования с использованием ускоренных электронов для стерилизации изделий медицинского назначения в ЛО.
Химический метод стерилизации
Разработка химических методов стерилизации изделий медицинского назначения во многом обязана широкому внедрению в медицинскую практику эндоскопического оборудования, разнородные материалы которого не выдерживают высоких температур.
Химическая стерилизация подразделяется на стерилизацию растворами (веществами) и стерилизацию газами (газовая стерилизация), а также плазменную стерилизацию.
В настоящее время для газовой стерилизации используются химические соединения, обладающие спороцидным действием, среди них окись этилена, бромистый метил, смесь окиси этилена и бромистого метила (смесь ОБ в соотношении 1:2,5) и формальдегид (рис.89).
Рис.89 Газовый стерилизатор (формальдегидный)
При стерилизации газами необходимо на строго определенном уровне поддерживать температуру, влажность, концентрацию газа, давление и экспозицию. Это возможно только при наличии оборудования с автоматизированным прохождением цикла.
Спороцидное действие газа зависит от числа и вида микроорганизмов, оставшихся на поверхности изделий после предстерилизационной обработки. Микробные клетки, оставшиеся на поверхности объекта, уничтожаются сравнительно быстро. В случаях, когда микробные клетки находятся в слое белковых загрязнений, эффективность стерилизации будет сомнительной, так как клетки, не контактирующие с газом, могут сохранить жизнедеятельность. Отсюда совершенно очевидно, что все медицинские изделия перед проведением газовой стерилизации должны подвергаться тщательной предстерилизационной очистке.
Плазменная стерилизация
Рис.90 Плазмовый стерилизатор
Существует современный, эффективный, но весьма дорогой метод стерилизации – плазменная стерилизация в низкотемпературных плазменных стерилизаторах SPS (рис.90). Принцип работы этой аппаратуры основан на генерации плазмы непосредственно вокруг стерилизуемого материала. Стерилизующим агентом является 20 %-ный пероксид водорода. Пероксид водорода и плазма имеют большое преимущество – распадаются на нетоксичные продукты – воду и кислород, не оказывая вредного воздействия на окружающую среду.
Такая технология отличается максимально щадящим воздействием на конструкционные материалы медицинских изделий, что дает уникальные возможности для многократной стерилизации изделий, содержащих высококачественную оптику, электронику, а также изделий со специальными покрытиями или красками. Стерилизация проводится в сухой атмосфере при температуре 36°С – 50°С, что гарантирует сохранность инструментов и оборудования, чувствительного к повышенной температуре и влажности.
Данный метод стерилизации применяют как альтернативу низкотемпературной газовой стерилизации окисью этилена и стерилизации в парах формальдегида. Использование окиси этилена все более и более ограничивают из-за высокой токсичности стерилизующего агента и необходимости последующей длительной вентиляции стерилизованных изделий.
Химическая стерилизация растворами
Рис.91 Химическая стерилизация эндоскопов
Химическая стерилизация проводится растворами химических веществ путем полного погружения изделия в раствор на время стерилизационной выдержки, после чего изделие должно быть промыто стерильной водой.
Химический метод следует применять для стерилизации изделий, в конструкцию которых входят термолабильные материалы (эндоскопы, лапароскопы, гистероскопы и др.) (рис.91). Конструкция изделия должна позволять стерилизовать его растворами химических средств. При этом необходим хороший доступ стерилизующего средства и промывной жидкости ко всем стерилизуемым поверхностям изделия.
При стерилизации растворами химических средств используют стерильные ёмкости из стекла, металлов, термостойких пластмасс, выдерживающих стерилизацию паровым методом, или покрытые эмалью (эмаль без повреждений).
Температура растворов, за исключением специальных режимов применения перекиси водорода и средства Лизоформин 3000, должна составлять не менее 20°С для альдегидсодержащих средств и не менее 18°С – для остальных средств.
Современные химические стерилянты и режимы стерилизации
Стерилизацию проводят при полном погружении изделий в раствор, свободно их раскладывая. При большой длине изделия его укладывают по спирали. Разъёмные изделия стерилизуют в разобранном виде. Каналы и полости заполняют раствором. Во избежание разбавления рабочих растворов, используемых для стерилизации, погружаемые в них изделия должны быть сухими.
Стерильные изделия промываются после перекиси водорода в двух водах по 5 минут.
Промытые стерильные изделия после удаления остатков жидкости из каналов и полостей используют сразу по назначению или помещают (с помощью стерильных пинцетов, корнцангов) на хранение в стерильную стерилизационную коробку, выложенную стерильной простыней, на срок не более 3 суток.
Высокий риск реконтаминации, а также дороговизна стерилянтов позволяет использовать данный метод только для стерилизации медицинских изделий, сложных в своей конструкции.
Средства химической стерилизации
Для стерилизации изделий разрешены к применению средства отечественного и зарубежного производства из следующих основных химических групп соединений: поверхностно-активных веществ (ПАВ), окислителей, хлорсодержащих средств, средств на основе перекиси водорода, спиртов, альдегидов .
Средства, содержащие спирты . обладают свойством фиксировать загрязнения органического происхождения, что обуславливает необходимость предварительного отмыва загрязнённых изделий перед стерилизацией с соблюдением противоэпидемических мер.
Хлорсодержащие средства (клорсепт, нейтральный аналит и др.), а также большинство средств на основе перекиси водорода предназначены для стерилизации изделий из коррозионностойких металлов, а также других материалов – резин, пластмасс, стекла.
Химическая стерилизация растворами йодата инадуксусной кислоты вызывает сильную коррозию никелевых покрытий и латуни, из которой изготавливают много изделий (шприцевая арматура многоразовых шприцев, бужи, катетеры, зеркала). Коррозионное воздействие растворов перекиси водорода проявляется значительно слабее и практически сводится к потемнению никелевого покрытия и медленному разрушению латуни. При наличии каналов и других незащищённых участков перекись водорода приводит к значительному сокращению срока службы таких медицинских инструментов. При стерилизации изделий медицинского назначения допускается применение только медицинской перекиси водорода.
Более щадящим действием по отношению к материалам, из которых изготавливаются медицинские изделия, обладают альдегидсодержащие средства . Глутарал, Глутарал-Н, Бианол, Аламинол, Сайдекс, Гигасепт ФФ, Лизоформин 3000, Дезоформ, Альдазан 2000, Секусепт-форте, Септодор-Форте и др. Эти средства рекомендованы для изделий из стекла, металлов, резин, пластмасс, в том числе термолабильных. Недостатком многих средств из этой группы является их способность фиксировать органические загрязнения на поверхности и в каналах изделий. Во избежание этого изделия необходимо сначала подвергнуть качественной предстерилизационной очистке.
Контроль качества стерилизации
Качество и эффективность стерилизации зависят от многих факторов, один из них – контроль стерилизации.
В соответствии с инструктивно-методическими документами Минздрава РФ, для получения объективной оценки качества стерилизации ее контроль должен проводиться комплексно:- Проводится оператором, обслуживающим стерилизационное оборудование.
- Должен проводиться ежедневно при проведении каждого цикла стерилизации.
- Позволяет оперативно выявить и устранить отклонения в работе стерилизационного оборудования.
Недостаток. Оценивает действие параметров внутри камеры аппарата, а не внутри стерилизуемых упаковок и поэтому должен использоваться в комплексе с другими методами контроля.- Должен проводиться ежедневно при проведении каждого цикла стерилизации.
- Проводится с использованием химических индикаторов.
- Принцип действия химических индикаторов основан на изменении состояния индикаторного вещества или (и) цвета индикаторной краски при действии определенных параметров стерилизации, строго специфичных для каждого типа индикаторов, в зависимости от метода и режима стерилизации.
По принципу размещения индикаторов на стерилизуемых объектах различают два типа химических индикаторов: наружные и внутренние:
- Наружные индикаторы (ленты, наклейки) крепятся липким слоем на поверхности используемых упаковок (бумага, металл, стекло и т.д.) и удаляются впоследствии. Наружным индикатором могут являться также некоторые упаковочные материалы (например, бумажно-пластиковые мешки, рулоны), содержащие химический индикатор на своей поверхности.
- Внутренние индикаторы размещаются внутри упаковки со стерилизуемыми материалами вне зависимости от ее вида (бумажный пакет или металлический контейнер и др.). К ним относятся различные виды бумажных индикаторных полосок, содержащие на своей поверхности индикаторную краску.
О применении химических термотестов для контроля физической стерилизации (воздушным и паровым методом) говорилось выше.
2) Посев простерилизованного материала на стерильность и забор смывов на стерильность.
Биологический метод подтверждает эффективность выбранного режима стерилизации.
ЦСО – централизованные стерилизационные отделения – организованы во всех современных лечебных учреждениях (рис.92).
1. предстерилизационная очистка медицинского инструментария;
а) медицинского инструментария,
б) белья и перевязочного материала,
в) резиновых и латексных изделий.
Устройство ЦСО.
«Помещения ЦСО должны быть разделены на три зоны - грязная, чистая и стерильная. К грязной зоне относятся помещения приема и очистки изделий медицинского назначения, к чистой зоне относятся помещения упаковки, комплектации и загрузки в стерилизаторы. К стерильной зоне относятся: стерильная половина стерилизационной - автоклавной, склад стерильных материалов и экспедиция» (СанПиН 2.1.3.2630-10 Санитарно-эпидемические требования к организациям, осуществляющим медицинскую деятельность.)
Современное центральное стерилизационное отделение должно иметь 3 зоны: «грязную», «чистую» и «стерильную».
«Грязная» зона – это помещения, в которых находится использованный инструментарий и материалы; представлены комнатой для приема материала в контейнерах из отделений и двумя моечными помещениями – одно для непосредственно инструментов и материалов, а другое – для транспортных тележек, на которых осуществляется перевозка контейнеров по лечебному учреждению. «Грязная» зона сообщается с «чистой» только через моечные автоматы проходного типа и посредством закрывающегося передаточного окна (для передачи инструментов, продезинфицированных и высушенных вручную). В состав «грязной» зоны включены также гардероб для верхней одежды и санузлы общего пользования.
«Чистая» зона – это те помещения, что расположены непосредственно за мойками. Там находятся инструменты и материалы уже чистые, но еще не стерильные. К этим помещениям относятся комнаты упаковки и подготовки к стерилизации инструментов, подготовки и упаковки текстиля, изготовления перевязочных материалов, различные складские помещения и комнаты для персонала, одетого в спецодежду (халаты, головные уборы, специальная обувь). Вход в «чистую» зону осуществляется через санпропускник.
«Стерильная» зона – это, собственно, склад простерилизованного материала. Он отделен от «чистой» зоны проходными стерилизаторами. Это помещение особой чистоты, куда вход разрешен только через санпропускник, строго ограниченному персоналу, в специальной одежде. к примеру, обязательно в масках.
Помещения необходимо распланированы таким образом, чтобы потоки грязных, чистых и стерильных материалов и инструментов не пересекались.
Принципы работы ЦСО
Все изделия, поступающие в ЦСО, проходят несколько этапов технологической цепочки: прием и разборка, предстерилизационная обработка на различных типах оборудования, либо вручную, контроль качества предстерилизационной обработки, комплектование и упаковка, непосредственно стерилизация и выдача (доставка) в клинические отделения.
Наиболее ответственным моментом организации работы ЦСО является сохранение стерильности медицинских изделий при разгрузке из стерилизаторов, комплектовании их в стерильной зоне, при транспортировке и использовании в клинических отделениях.
Простерилизованные изделия в стерилизационных коробках должны оставаться в автоклаве в течение 1,5 –2 часов до полного остывания. Во время остывания не должно быть сквозняков в помещении и доступа холодного воздуха. ЦСО должна быть оборудована приточно-вытяжной вентиляцией.
При разгрузке стерилизатора исключается присутствие других сотрудников ЦСО, кроме персонала стерильной зоны.
Документация ЦСО
Основной перечень документов ЦСО: Паспорт ЦСО, Должностные инструкции заведующего, старшей медсестры, медицинской сестры ЦСО, санитарки, Журнал учета качества ПСО, Журнал контроля работы стерилизаторов воздушного, парового (автоклава), Журнал исследований на стерильность, Инструкция по технике безопасности при работе в стерилизационных, Журнал инструктажа на рабочем месте, Памятка-рекомендация по правильной загрузки парового стерилизатора, Журнал регистрации и контроля бактерицидной установки, Журнал учёта генеральных уборок, Журнал учёта аварийной ситуации, травм медперсонала на рабочем месте.
учета качества предстерилизационной обработки
Начат "____"___________19___г. Окончен "_____"___________19__г.
и т.д. до конца страницы
РАБОЧИЙ ЖУРНАЛ
исследований на стерильность ф. N 258/у
Начат ". " ________ 19. г. Окончен ". " _________ 19. г.
Методы отбора образцов и их лабораторные
исследования проводятся в соответствии со
следующей нормативно-технической документацией
(НТД перечислить):
1. ________________________________________
2. ________________________________________
3. ________________________________________
4. ________________________________________
Учреждение,
место
взятия
материала
Обработка
материала и
дата посева
в аэробных
условиях
Дата
окончания
исследования.
Подпись лица,
провод. исслед.
в анаэробных условиях
и т.д. до конца страницы.
Преимущества стерилизации в ЦСО
Недостатки децентрализованной стерилизации
К сегодняшнему дню в российских лечебных организациях сложилось несколько форм организации стерилизации: децентрализованная. централизованная (осуществляемая в ЦСО) и смешанная.
Децентрализованная (локальная, кабинетная) стерилизация– организация стерилизации на рабочих местах вручную либо в специально отведенных для этого помещениях (стерилизационных) в разных отделениях медицинского учреждения. ПСО изделий проводится также вручную.
База данных защищена авторским правом ©zubstom.ru 2015
обратиться к администрации