







Категория: Бланки/Образцы
и учреждениях здравоохранения
5.1. Аптечные учреждения, осуществляющие отпуск МИБП гражданам, ведут учет поступления и расхода МИБП. Для этого должны быть в наличии следующие документы:
- журнал учета поступления и расхода МИБП;
- накладные на приобретение МИБП;
- инструкции по применению МИБП на русском языке;
- акты об уничтожении МИБП;
- акты проверки условий хранения, учета и расходования МИБП специалистами центров госсанэпиднадзора.
VI. Организация отпускагражданам МИБП в аптечных учреждениях
и учреждениях здравоохранения и применения их
в лечебно - профилактических учреждениях
6.1. МИБП отпускаются гражданам по рецепту врача лечебно - профилактического учреждения (независимо от форм собственности и ведомственной принадлежности).
6.2. Отпуск МИБП гражданам возможен при условии доставки препарата до места непосредственного использования с соблюдением "холодовой цепи" в термоконтейнере или термосе.
6.3. Гражданам выдается необходимое количество доз вакцины в соответствии с рецептом, вакцина снабжается инструкцией по применению на русском языке. На упаковке проставляется дата и время отпуска препарата.
6.4. Работник аптеки объясняет покупателю необходимость доставки препарата в лечебно - профилактическое учреждение в минимальные сроки (не более 48 часов) после приобретения препарата в условиях хранения последнего в термоконтейнере или холодильнике.
6.5. Приобретенная в аптечном учреждении вакцина используется в прививочных кабинетах ЛПУ, детских дошкольных образовательных учреждениях, медицинских кабинетах общеобразовательных учебных учреждений (специальных образовательных учреждениях), здравпунктах и других медицинских учреждениях, независимо от форм собственности, имеющих лицензию на проведение иммунопрофилактики при строгом соблюдении условий хранения и транспортировки.
VII. Уничтожение мибп7.1. МИБП подлежат уничтожению:
- с истекшим сроком годности;
- хранившиеся с нарушением "холодовой цепи";
- с изменившимися внешними свойствами, не обозначенными в инструкции (наличие хлопьев, инородных предметов, изменение цветности и прозрачности и др.).
7.2. Уничтожение МИБП проводится в том же помещении, где они хранятся.
7.3. Ампулы и флаконы с инактивированными и рекомбинантными вакцинами, иммуноглобулинами, гетерологическими сыворотками, живой коревой, паротитной и краснушной вакцинами вскрываются, содержимое выливается в раковину, стекло выбрасывается в емкость для мусора без дополнительного обеззараживания.
7.4. Ампулы и флаконы с другими живыми вакцинами после вскрытия помещают в 3%-ный раствор хлорамина на 1 час (вакцины БЦЖ и БЦЖ-М в 5%-ный раствор или 3%-ный раствор перекиси водорода), затем выливают в раковину, стекло выбрасывают в емкость для мусора.
7.5. Для обеззараживания живых вакцин и загрязненных ими поверхностей используются дезинфекционные средства в соответствии с инструкцией по применению.
VIII. Условия соблюдения техники безопасности8.1. В случае повреждения емкости, содержащей вакцинный препарат (стеклянные флаконы, ампулы и пр.), ее уничтожают в соответствии с пунктами 7.3 - 7.5 настоящих правил.
8.2. При попадании вакцинного материала на слизистые оболочки глаз их промывают большим количеством воды.
8.3. В случае повреждения кожных покровов рану обрабатывают настойкой йода.
8.4. Мебель или участки пола, загрязненные вакцинным препаратом, обрабатываются 3%-ным раствором хлорамина или другими дезинфектантами в соответствии с инструкцией по применению.
8.5. При уборке осколков стекла необходимо пользоваться щетками, пинцетом и совком.
УЧЕТА ПОСТУПЛЕНИЯ И РАСХОДА ВАКЦИНЫ
Официально распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль".
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставкиПравила устанавливают основные требования к транспортированию, хранению, отпуску аптечными учреждениями и учреждениями здравоохранения медицинских иммунобиологических препаратов, используемых для иммунопрофилактики инфекционных болезней; применению МИБП в лечебно-профилактических учреждениях; организации уничтожения МИБП в случае невозможности их использования.
3.3.2. МЕДИЦИНСКИЕ ИММУНОБИОЛОГИЧЕСКИЕ ПРЕПАРАТЫ
Санитарно-эпидемиологические требования
к условиям транспортирования, хранению
и отпуску гражданам
медицинских иммунобиологических препаратов,
используемых для иммунопрофилактики,
аптечными учреждениями
и учреждениями здравоохранения
Санитарно-эпидемиологические правила
СП 3.3.2.1120-02
1. Разработаны: Департаментом Госсанэпиднадзора Минздрава России (к.м.н. Г.Ф. Лазикова, к.м.н. Н.А. Кошкина), Федеральным центром Госсанэпиднадзора Минздрава России (А.А. Ясинский, В.Н. Садовникова, Л.Н. Костина), Центром Госсанэпиднадзора в г. Москве (к.м.н. И.А. Храпунова).
2. Утверждены 4 апреля 2002 г. и введены в действие постановлением Главного государственного санитарного врача Российской Федерации Г.Г. Онищенко от 10 апреля 2002 г. № 15 с 1 августа 2002 г.
3. Зарегистрированы в Министерстве юстиции Российской Федерации 8 мая 2002 г. Регистрационный номер 3419.
4. Введены впервые.
Федеральный закон Российской Федерации
«О санитарно-эпидемиологическом благополучии населения»
«Государственные санитарно-эпидемиологические правила и нормативы (далее - санитарные правила) - нормативные правовые акты, устанавливающие санитарно-эпидемиологические требования (в т. ч. критерии безопасности и (или) безвредности факторов среды обитания для человека, гигиенические и иные нормативы.), несоблюдение которых создает угрозу жизни или здоровью человека, а также угрозу возникновения и распространения заболеваний» (статья 1).
«Соблюдение санитарных правил является обязательным для граждан, индивидуальных предпринимателей и юридических лиц» (статья 39).
«За нарушение санитарного законодательства устанавливается дисциплинарная, административная и уголовная ответственность» (статья 55).
Федеральный закон Российской Федерации
«Об иммунопрофилактике инфекционных болезней»
№ 157-ФЗ от 17 сентября 1998 г.
«Отпуск гражданам медицинских иммунобиологических препаратов, используемых для иммунизации, проводится по рецептам врачей аптечными организациями и организациями здравоохранения в порядке, установленном федеральным органом исполнительной власти в области здравоохранения» (статья 12).


Министерство здравоохранения Российской Федерации
ГЛАВНЫЙ ГОСУДАРСТВЕННЫЙ САНИТАРНЫЙ ВРАЧ
РОССИЙСКОЙ ФЕДЕРАЦИИ
На основании Федерального закона «О санитарно-эпидемиологическом благополучии населения» от 30 марта 1999 г № 52-ФЗ и Положения о государственном санитарно-эпидемиологическом нормировании, утвержденного постановлением Правительства Российской Федерации от 24 июля 2000 г. № 554
Ввести в действие санитарно-эпидемиологические правила «Санитарно-эпидемиологические требования к условиям транспортирования, хранению и отпуску гражданам медицинских иммунобиологических препаратов, используемых для иммунопрофилактики, аптечными учреждениями и учреждениями здравоохранения. СП 3.3.2.1120-02», утвержденные Главным государственным санитарным врачом Российской Федерации 4 апреля 2002 г. с 1 августа 2002 г.
1. Область применения
3. Условия транспортирования МИБП в аптечные учреждения и учреждения здравоохранения
4. Условия хранения МИБП в аптечных учреждениях и учреждениях здравоохранения
5. Учет МИБП в аптечных учреждениях и учреждениях здравоохранения
6. Организация отпуска гражданам МИБП в аптечных учреждениях и учреждениях здравоохранения и применения их в лечебно-профилактических учреждениях
7. Уничтожение МИБП
8. Условия соблюдения техники безопасности
Термины и определения
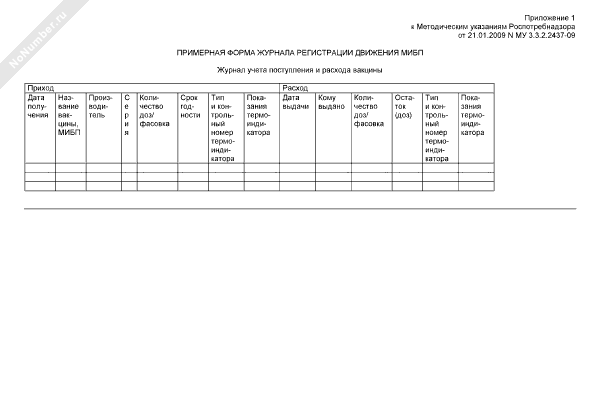
Приложение 1. Журнал учета поступления и расхода вакцины
Приложение 2. Журнал регистрации температурного режима холодильника
Количество покупок: 20580
Постановлением Главного государственного санитарного врача РФ от 17.02.2016 г. N 19 «Об утверждении санитарно-эпидемиологических правил СП 3.3.2.3332-16 «Условия транспортирования и хранения иммунобиологических лекарственных препаратов» утвержденжурнал учета движения ИЛП (журнал учета движения иммунобиологических лекарственных препаратов).
Форма журнала учета движения иммунобиологических лекарственных препаратов (ИЛП) утверждена (Приложение №3 к СП 3.3.2.3332-16) и действует в настоящее время. Аптечные учреждения, осуществляющие отпуск ИЛП гражданам, обязаны вести учет поступления и расхода ИЛП по указанной форме - пп. 8.1 СП 3.3.2.3332-16.
Порядок ведения журнала учета движения ИЛП в аптеке:
На всех уровнях «холодовой цепи» в специальном журнале (Приложение №3 к СП 3.3.2.3332-16) проводится регистрация поступления и отправления ИЛП в организации с указанием наименования производителя препарата, его количества (для вакцин и растворителей к ним - в дозах), серии, контрольного номера, срока годности, даты поступления (отправления), организации-поставщика, показаний термоиндикаторов и их идентификационных номеров, фамилии, имени, отчества (при наличии) ответственного работника, осуществляющего регистрацию.
Документ содержит как бланк журнала, так и образец для заполнения.
Внешний вид документа:

Вы можете получить платную индивидуальную консультацию и заполнение ваших документов экспертами сервиса МедИнфо24.
Отправляйте заявку или звоните по телефону: +7 (904) 866-01-00 .
Услуги предоставляются с момента оплаты до получения заключения или лицензии.
О гарантиях Мединфо24
Спасибо, журнал очень пригодился при проверке. Долго искал в интернете, но нашёлся только этом сайте.
Аптека №22 "Здрава"
Антон из службы поддержки очень помог: вовремя проконсультировал во время открытия аптеки. Премного благодарен, успехов вам.
Журнал регистрации движения МИБП.
Журнал регистрации движения МИБП по сути является документом, подтверждающим приход и расходование вакцин и иммунобиологических препаратов в медицинском учреждении (аптеке).
При поступлении МИБП в Журнале регистрации, помимо даты поступления и количества, фиксируется наименование, номер акта производителя, единицы измерения вещества, серия и срок его годности. Снимаются показания термоиндикатора и указывается его тип и контрольный номер.
В расходной части фиксируются выдачи препаратов на основании расходных документов, с указанием данных о веществе, как и в приходной части документа (исключая название вакцины или МИБП). Обязательно указывается получатель препарата.
Показания термоиндикатора снимаются для подтверждения соблюдения во время перевозки препаратов температурного режима, необходимого для вакцин и МИБП. Контрольный номер подтверждает факт регистрации и разрешение на использование.
Графы для заполнения Журнала регистрации движения МИБП:
В магазине Сити Бланк вы покупаете Журнал регистрации движения МИБП в альбомном формате. Приходная и расходная часть документа занимают один разворот. Количество страниц определяется покупателем.
Также предлагаем модифицировать обложку, заказав твердый переплет, выполняемый с применением заменителя кожи. Такая обложка презентабельна и удобна в использовании. На ее лицевой стороне возможно выполнение тиснения по тексту заголовка.
Для Журнала регистрации движения МИБП в мягкой обложке магазин Сити бланк предлагает ламинацию. Такой способ защиты издания экономичен и эффективен для защиты журнала от истирания и влаги.
Медицинская документация является носителем отображенной в ней информации медицинского характера в текстовом виде. В данном разделе представлен такой вид документации, как медицинские журналы по разным направлениям.
Медицинские журналы должны содержать реквизиты учреждения для его идентификации, предназначаются для передачи и сохранения информации. Это официальные документы, при определенных условиях, способные приобретать юридическую силу.
Медицинские журналы для регистрации данных могут использоваться для записи самых разных сведений о пациентах. Так, можно зафиксировать данные о состоянии органов и тканей, результаты исследований или анализов, назначенное лечение и пр. Данная документация также может содержать информацию о состоянии техники в медицинском учреждении, о наличии и движении препаратов, о количестве инструментария, о проведении дезинфекций или уборок помещений.
Часть форм предназначена исключительно для аптек, СЭС, АХО, роддомов. Полный перечень журналов по категориям можно найти здесь. В нашем каталоге можно подобрать печатную продукцию для любой отрасли медицины. Помимо журналов мы предлагаем также карты и бланки актуальных форм.
Безответственное отношение к ведению медицинских журналов может повлечь неприятные последствия. Данные документы могут использоваться в случае инициирования пациентом или лицами представляющими его интересы разбирательств. Любой медицинский журнал, как единица первичной документации, удостоверяет те или иные события, фиксирует факты свершившиеся в пределах правового поля.
Многие из представленных в каталоге журналов имеют утвержденную форму. При изготовлении такой продукции специалисты нашей типографии строго соблюдают установленные требования. В нашем интернет-магазине вы можете приобрести продукцию типографии Сити Бланк как унифицированного, так и вольного формата.
При покупке журнала обратите внимание на характеристики товара. Вы можете сделать любые нужные модификации при необходимости. Измените объем журнала в большую или меньшую сторону, закажите изделие в твердой обложке, воспользуйтесь возможностью нанесения ламинирующего покрытия или прошивки изделия по требованиям правил делопроизводства.
В наше время многие частные медицинские учреждения имеют свою символику. Например логотип. У нас вы можете заказать нанесение индивидуальной символики вашей организации, а также названия и прочих реквизитов на обложку или внутренние страницы издания. О дополнительных требованиях необходимо сообщить менеджеру. Например, можно указать свои пожелания при оформлении покупки.
Журнал регистрации движения МИБП

Журнал регистрации движения МИБП
ОПИСАНИЕ: Форма журнала учета поступления и расхода вакцины соответствует Приложению N 1 Постановления Главного государственного санитарного врача РФ от 10.04.2002 N 15 (ред. от 18.02.2008) "О введении в действие санитарно-эпидемиологических правил СП 3.3.2.1120-02" (вместе с "СП 3.3.2.1120-02. 3.3.2. Медицинские иммунобиологические препараты. Санитарно-эпидемиологические требования к условиям транспортировки, хранению и отпуску гражданам медицинских иммунобиологических препаратов, используемых для иммунопрофилактики, аптечными учреждениями и учреждениями здравоохранения. Санитарно-эпидемиологические правила", утв. Главным государственным санитарным врачом РФ 04.04.2002) (Зарегистрировано в Минюсте РФ 08.05.2002 N 3419)
Графы журнала учета поступления и расхода вакцины :
Приход
1. Дата получения
2. Название вакцины
3. Количество
4. Серия, контрольный номер
5. Срок годности
6. Страна и фирма производитель
7. Условия транспортировки, показания термоиндикатора
Расход
8. Дата выдачи
9. Кому выдано
10. Кол-во выданной вакцины
11. Серия и контрольный номер
12. Остаток
Ворос аптеки:
Согласно СП 3.3.2.1120-02 к условиям транспортирования, хранения и отпуска аптечными учреждениями иммунобиологических препаратов предусмотрено при разгрузке МИБП фиксировать в журнал учета движения МИБП дату поступления, наименование препарата, его количество, серию, срок годности, фирму-производителя, показания термоиндикаторов. Согласно приложению N 1 данного СанПиН этот журнал называется "Журнал учета поступления и расхода вакцин ". Требуется ли в таком же журнале регистрировать бактериофаги, интерфероны, бифидумбактерин, аципол и т.д. или это касается исключительно вакцин (соответственно названию журнала )? Кроме того, МИБП требуется подвергать визуальному контролю 1 раз в месяц. Каким образом регистрировать результаты данного контроля? Существует ли определенная форма журнала или это оформляется протоколом осмотра?
Ответ Юриста: В соответствии с пунктом 5.1 Санитарно-эпидемиологических правил "Санитарно-эпидемиологические требования к условиям транспортировки, хранению и отпуску гражданам медицинских иммунобиологических препаратов, используемых для иммунопрофилактики, аптечными учреждениями и учреждениями здравоохранения" СП 3.3.2.1120-02 (в ред. от 18.02.2008) аптечные учреждения, осуществляющие отпуск МИБП гражданам, должны вести учет поступления и расхода МИБП. При этом указывается, что в аптечной организации для этого должен быть в наличии журнал учета поступления и расхода МИБП .
Указанными Правилами перечень факторов и параметров, подлежащих отражению в журнале учета. не установлен. Форма журнала учета приведена в Приложении N 1 к Правилам только для вакцин.
В то же время в Правилах не оговорено, что порядок учета для разных групп медицинских иммунобиологических препаратов может или должен быть различным. По нашему мнению, учет любых МИБП, поступающих в аптечную организацию должен вестись по форме, установленной в Приложении N 1 к Правилам.
Согласно пункту 4.12 СП 3.3.2.1120-02 медицинские иммунобиологические препараты следует в процессе хранения подвергать выборочному визуальному контролю не реже, чем один раз в месяц. Требование фиксации такого контроля в каких-либо журналах или актах (протоколах) указанными Правилами не установлено, а также не установлен и порядок такой фиксации. В то же время, во избежание претензий со стороны контрольно-надзорных органов в ходе возможных проверок порядка хранения МИБП рекомендуем вести учет такого контроля в произвольной форме, определяемой локальным актом аптечной организации.
© ООО «Центр гигиены, санитарии, экологии населения» 2007-2014.
Адрес:г. Тула, ул. Немцова, д.38а, оф.5