






Категория: Бланки/Образцы
90 Sr-β-излучатель с периодом полураспада 28,6 лет. В результате распада 90 Sr образуется 90 Y, тоже β-излучатель с периодом полураспада 64,2 ч.
Выпадающие на поверхность Земли изотопы стронция мигрируют по биологическим цепочкам и, в конце концов, могут поступить в организм человека.
Степень и скорость всасывания стронция из желудочно-кишечного тракта зависит от того, в состав какого химического соединения он входит, от возраста человека и функционального состояния организма, от состава пищевого рациона. Так, у лиц молодого возраста стронций всасывается быстрее и полнее. Увеличение содержания в диете солей кальция снижает всасываемость соединений стронция. При потреблении молока всасываемость стронция повышается. В разных условиях всасываемость стронция из ЖКТ колеблется от 11 до 99%.
Всосавшийся стронций активно включается в минеральный обмен. Являясь аналогом кальция, радиоактивный стронций депонируется преимущественно в костях и в костном мозге (критические органы).
Выводится стронций с калом и мочой. Эффективный период полувыведения составляет 17,5 лет.
В ранние сроки после поступления 90 Sr в большом количестве наблюдаются изменения в органах, через которые он поступает или выводится: слизистые оболочки рта, верхних дыхательных путей, кишечник. Позднее нарушаются функции печени. При ингаляционном поступлении малорастворимых соединений стронция изотоп может достаточно прочно фиксироваться в легких, которые в этих случаях вместе с дыхательными путями являются критическими органами. Однако в отдаленные сроки и после ингаляционного поступления критическими органами становятся кости и костный мозг, в которых депонируются до 90% всей активности.
В процессе реакции кроветворной ткани на стронций в течение длительного времени морфологический состав крови меняется мало. Лишь при поступлении больших количеств развивается и прогрессирует цитопения. Тяжелых случаев поражения с острым или подострым течением у человека не наблюдали.
При длительном поступлении стронция и подостром течении лучевой болезни постепенно развивается анемия, наблюдаются угнетение спермато- и овогенеза, нарушения иммунитета, функции печени и почек, нейроэндокринной системы, сокращается продолжительность жизни.
В отдаленные сроки развиваются гипер- или гипопластические процессы в костном мозге, лейкозы, саркомы кости. Реже наблюдаются новообразования в гипофизе и других эндокринных органах, в яичниках, молочной железе.
Большой период полураспада 90 Sr определяет длительное сохранение высоких уровней заражения территорий и объектов среды после загрязнения этим радионуклидом.
Среди продуктов ядерного деления присутствует и 89 Sr, который также является β-излучателем. Однако период полураспада 89 Sr короче - 53 сут, поэтому степень радиоактивного загрязнения объектов в этом случае снижается гораздо быстрее.
Радиоактивные изотопы стронция 89§г и 908г попадают в окружающую среду при испытаниях ядерного оружия в атмосфере, вследствие утечек на атомных электростанциях, а также из-за аварий на заводах по переработке ядерного топлива. Эти изотопы присутствуют в воде и почве на территориях восточно-уральского радиоактивного следа, образовавшегося после известных промышленных катастроф [7]. Период полураспада 89Бг составляет 50,5 суток, а 908г — 28,5 лет. Оба изотопа распадаются, испуская бета-излучение. В отличие от других радионуклидов обнаружение изотопов стронция затруднено, поскольку при своем распаде они не испускают гамма-лучи. Обнаружение этих радиоизотопов в воде связано с большими трудностями.[. ]
Радиоактивный Бг-90 крайне опасен для человека и животных. По химическим свойствам он похож на кальций и поэтому, попав в организм, накапливается в костях и оказывается в опасном контакте с костным мозгом — кровеносной тканью.[. ]
Радиоактивный изотоп кальция-45 применяют для определения способов размещения извести в почве. В опытах с клевером установлено, что он развивается лучше и дает более высокий урожай в том случае, если хотя бы небольшое количество извести было внесено вблизи семян. Это обеспечивает лучшее начальное развитие молодых растений, а в раннем возрасте клевер сильнее всего страдает от кислотности. Окрепнувшие молодые растения легче переносят в дальнейшем кислую реакцию. Следовательно, небольшие дозы извести не имеет смысла глубоко заделывать в почву. Если малую дозу извести запахать плугом, то верхний слой почвы, где прорастают семена, останется кислым и всходы могут погибнуть, не образовав достаточно длинных корешков, способных дойти до известкованного слоя. Желательнее всего вносить известь вдоль рядка, заделывая ее узкой полосой на глубину пахотного горизонта. При этом и меченого кальция в растение поступает больше и развитие его бывает лучше.[. ]
Кальций является химическим аналогом стронция, в том числе 908г, который появляется в почве при радионуклидном ее загрязнении. Обогащение почвы Са2+ путем известкования способствует уменьшению поступления 908г в растения. В связи с этим известкования рекомендуют проводить в зонах загрязнения радиоактивными выпадениями.[. ]
Стронций радиоактивный (898г, и др.) — искусственные радиоактивные изотопы С. образующиеся при делении урана. Долгоживущий радионуклид 908г (период полураспада — 27,7 года) — один из важных компонентов радиоактивного загрязнения биосферы. Попадая в окружающую среду включается, гл. обр. вместе с кальцием, в процессы обмена веществ в организмах. При оценке загрязнения биосферы принято рассчитывать отношение 908г/Са в стронциевых единицах (1 с.е. — 1 мкКи 908г на 1 г Са). В организмы животных и человека 908г поступает в основном с молоком и рыбой и накапливается преимущественно в костях. При длительном его поступлении могут развиваться лейкемия и рак костей. Сокращение испытаний ядерного оружия привело к резкому снижению содержания 908г в атмосфере и подвижных его форм в почве. Тетраэтилсвинец (ТЭС, (С2Н5)4РЬ) — жидкость, пары которой в малых концентрациях имеют запах фруктов, в больших — неприятный запах. В виде этиловой жидкости (смесь ТЭС с галогенопроизводными углеводородов, в которую добавлены краситель и антиокислитель) используется в качестве антидетонаци-онной присадки к бензину. Легко проникает через кожу. ПДК в воздухе — 0,000003 мг/м3. См. также Свинец.[. ]
Количество радиоактивных изотопов, которые включаются в пищевые цепи и в конце концов попадают в организм человека, определяется не только тем, сколько их выпало из воздуха (что, как уже отмечалось, непосредственно зависит от количества атмосферных осадков), но также структурой экосистемы и природой ее биогеохимических циклов. В общем в малокормных местообитаниях большая доля осадков будет входить в пищевые цепи. В богатой среде высокая скорость обмена и большая запасающая емкость почвы или донных отложений обеспечивают такое разбавление осадков, что в растения они попадают в относительно небольшом количестве. Подушковидная растительность тощих почв, такая, как моховые болота, заросли вереска, сообщества на выходах гранита, альпийские луга и тундры (и эпифиты в тропических экосистемах), действует как ловушка для осадков, ускоряя их потребление животными (Рассел, 1965), подобно тому как это происходит в дет-ритных пищевых цепях. Два примера такого рода представлены в табл. 60 и 61. В Англии овцы, пасущиеся на возвышенных местах, накапливают в костях в 20 раз больше стронция-90, чем овцы, пасущиеся в долинах, потому что для высоких пастбищ характерны низкое содержание кальция и подушковидная растительность (табл. 60).[. ]
Этот элемент имеет радиоактивный изотоп. Он поступает в окружающую среду с утечками из ядер-ных реакторов вместе с кальцием. Попадая в организм, может накапливаться в костных тканях и оказывать канцерогенное воздействие.[. ]
Обсуждение проблемы радиоактивных загрязнений атмосферного воздуха мы ограничиваем рассмотрением лишь тех радиоактивных веществ, которые могут присутствовать в воздухе в виде газов и аэрозолей, испускающих ионизирующие альфа- и бета-частицы, гамма-лучи, нейтроны и другие кванты, обладающие высокой энергией. С практической точки зрения радиоактивными изотопами, представляющими наибольшую опасность, являются йод-131, фосфор-32, кобальт-60, стронций-90, углерод44, сера-35, кальций-45, золото-198, радий-226 и уран, причем они чаще содержатся в воздухе в соединениях с другими веществами, чем в виде элементов (US National Bureau od Standards, 1953).[. ]
В модели круговорота кальция и цезия, основанные на структуре и измеренных интенсивностях их потоков в дождевом тропическом лесу Пуэрто-Рико, вводили нарушение, состоявшее в удвоении устойчивого притока биогенов на срок 10 лет. Возвращение систем к разновесному состоянию имитировалось для последующего 30-летнего периода (Jordan et al. 1972). Лишний цезий быстро вымывался из сообщества (рис. 21.12). Это обстоятельство было подтверждено и изучением периода полураспада радиоактивного цезия-137 из атмосферных осадков; изотоп в основном выводился из экосистемы дождевого тропического леса при опадении листвы (Kline, 1970). В отличие от этого модель круговорота кальция показала гораздо меньшую упругость (рис. 21.12).[. ]
Таким методом [343] удалялись радиоактивные барий, стронций, скандий, цирконий — ниобий на 95—99%. Для освобождения воды от стронция необходим избыток соды и извести. При стехиометрическом количестве добавляемых реагентов удаление стронция происходит на 75, при 100 мг/л избытка—на 85,3 и при 200 мг/л—на 99,4%. Лабораторная проверка показала снижение концентрации ионов 5г2+ более чем на 99% при многоступенчатом известково-содовом умягчении с добавкой солей кальция и затравки ¦в виде готовых (образовавшихся) кристаллов.[. ]
Почвы обладают естественной радиоактивностью в связи с содержанием радиоактивных элементов (уран, торий, радий) или изотопов (калий, кальций, рубидий и др.). Искусственная радиоактивность обусловлена поглощением радиоактивных изотопов, образующихся при ядерных взрывах и при промышленном использовании ядерной энергии.[. ]
Эффективным способом борьбы с радиоактивным загрязнением является закрепление радионуклидов органическим веществом с образованием нерастворимых комплексов (хелатов). В большинстве почв повышение pH, количества обменного калия и кальция способствует сорбции радионуклидов (например, стронция). Глинистые минералы хорошо фиксируют такие радионуклиды, как стронций, цезий.[. ]
При соприкосновении раствора соли кальция, содержащей радиоактивный изотоп Са45, с почвой, насыщенной кальцием, радиоактивность раствора понижается вследствие того, что радиоактивный кальций равномерно распределяется между раствором и кальцием, находящимся в поглощенном состоянии. Зная содержание кальция в растворе и измерив его радиоактивность, по разности в радиоактивности исходного и равновесного раствора рассчитываем содержание кальция в поглощенном состоянии. Этот простой расчет сразу дает количество кальция в поглощенном состоянии, способного к обмену. Результаты такого расчета для опытов с образцами трех почв, покровным суглинком и бентонитом приведены в табл. 2.[. ]
В случае солонца отклонение вызвано тем, что кальций раствора легко обменивается на натрий, находящийся в поглощенном состоянии. Ошибка, вызванная изменением концентрации кальция в растворе, не компенсируется неполнотой вытеснения натрия. Для бурой горно-лесной почвы отклонение вызвано тем, что барий вытесняет водород энергичнее, чем кальций. Кроме того, здесь так же, как и в предыдущем случае, не сбалансированы ошибки, связанные с уменьшением концентрации кальция в растворе. По этим причинам для почв, содержащих в обменном состоянии помимо калбция и магния также и другие катионы (натрий, водород), радиоактивный метод не пригоден.[. ]
В результате опытов, проведенных по удалению радиоактивного стронция, оказалось, что последний может соосаждаться с карбонатом кальция за счет многократных добавок хлористого кальция и рециркуляции образовавшегося осадка. Считают, что стронций удаляется за счет образования либо смешанных кристаллов кальцита-стронцианата (без подогрева), либо арагонита-стронцианата (при подогреве). При однократном прохождении через содово-известковый водоумягчитель концентрация радиостронция снижается на 50, при повторном — до 90% .[. ]
Ньюел (Newell) и сотрудники [4] предлагают очищать радиоактивные сточные воды от промывки ядерных реакторов химическим путем, применяя для этого следующие добавки коагулянтов: хлористый кальций — 300 мг/л, силикат натрия 20 мг/л, хлористое железо (III) 60 мг /л, раствор едкого натра с pH = 12,0.[. ]
Как видно из данных табл. 4, величины емкости по радиоактивному методу несколько ниже по сравнению с данными, полученными по методу Бобко-Аскинази. Это вполне понятно, если учесть, что величины емкости по кальцию также обычно бывают ниже, чем по барию, как это имеет место в методе Бобко-Аскинази. В двух случаях имеются значительные отклонения от метода Бобко-Аскинази: для солонца и бурой горно-лесной почвы, Для солонца данные завышены, а для горно-лесной — занижены.[. ]
Во-вторых, радионуклиды, определяющие естественную радиоактивность углей (торий, уран, калий) не обладают такими опасными для живого свойствами, какими, например, обладают радиоактивный йод (накапливающийся в щитовидной железе), стронций-90 (замещающий в скелете кальций), или весьма ради ото ксичный плутоний. Живое приспособлено к их присутствию в биосфере в ходе сотен миллионов лет эволюции планеты. В отличие от этого, многие радионуклиды, возникающие на АЭС, как, например, плутоний и технеций, являются совершенно чуждыми для живого.[. ]
Много интересного дало и применение меченого фосфора, кальция, серы, калия и других элементов. Внесение в почву суперфосфата, содержащего радиоактивный изотоп фосфора-32 и хлористого калия, содержащего радиоактивный изотоп калия-42, подтвердило крайне слабое передвижение этих растворимых в воде солей в почве из-за энергичного поглощения их составных частей -кальция, фосфора, калия — почвенными мельчайшими частицами. Тем самым еще раз подчеркнута важность глубокого внесения в почву основной массы этих удобрений, особенно в засушливых районах. В противном случае использование их растениями резко понижается.[. ]
Хороших результатов дезактивации можно добиться при осаждении радиоактивных изотопов фосфатом кальция. Многие исследователи избрали этот реагент ввиду того, что число нерастворимых фосфатных соединений гидратов окисей, образующихся при коагулянтов. Хлопья фосфата кальция могут образовываться в растворе с высоким pH — условие, благоприятное для адсорбции некоторых ионов.[. ]
Другой весьма интересной физико-химической возможностью борьбы с радиоактивной загрязненностью является система агротехнических мер, направленных против поглощения радиоактивного стронция корневой системой. В этом плане можно упомянуть: а) работы, в которых имеется в виду снижение поглощения специальными методами обработки почв, их эффективность оказалась весьма малой; б) работы, в которых предполагается ослабление эффекта поглощения корнями растений путем известкования почв карбонатами и сульфатами для создания высокой концентрации ионов Са2+ и удовлетворения потребностей растений в щелочноземельных элементах за счет кальция. В том же направлении усиления сорбционных свойств почвы и более прочного закрепления поглощенных продуктов радиоактивного распада действуют внесенные в почву органические удобрения или, еще лучше, комбинации из извести и органических удобрений. Анализ показал, что при этом можно уменьшить содержание 908г в соломе в 2-3 раза и в зерне в 3-5 раз. Внесение калия в комбинации с различными удобрениями приводит к снижению 137Св в урожае. Данный метод особенно эффективен на легких, кислых почвах, бедных кальцием [59].[. ]
Срезанные ветки помещали на У2 питательной смеси Кнопа, содержавшей радиоактивный изотоп кальция (Са45). Затем через определенные промежутки времени проводились определения содержания Са45 в ветках. Часть вето« исследовали до обособления бутонов, вторую часть — после обособления бутонов (табл. 1).[. ]
Из этих элементов самый тяжелый — железо (атомный вес 55,84), перед ним кальций (атомный вес 40,08). В этот список не включены радиоактивные элементы наиболее тяжелые, как радий или актиний (атомные веса 225,97 227), неизбежные для жизни, так как количество их есть характерный видовой признак [39], но они в химические соединения тел организмов не входят, а являются для живого вещества источником энергии.[. ]
Авторы проверяли точность определения, насыщая т аким же способом корни радиоактивным цезием; хлорид кальция вытеснял его на 97 %. Следовательно, чувствительность метода достаточная. Пользуясь меченым цезием, они показали, что у кукурузы наибольшей емкостью поглощения обладает растущая часть корня на расстоянии около 2 мм от его кончика; у корней кормовых бобов максимальная емкость поглощения приходилась на ответвления, размещенные в 0,8—2 см от кончика. У ячменя самая высокая емкость катионного поглощения наблюдалась в зоне развития корневых волосков. Заметим, что максимальная величина отрицательного электрического заряда корней также находится в зоне развития корневых волосков.[. ]
Таким образом, результаты этих двух опытов давали основание предполагать, что кальций, освобождающийся в результате разложения растения при наличии грунта, проникает в его толщу. Для подтверждения этого предположения в нескольких местах из песчаного грунта с примесью ила по всей 5-см толщине его были извлечены тонкой стеклянной трубкой монолиты, в которых по слоям через 1 см определялась радиоактивность грунта. Оказалось, что кальций содержится во всей толще ила, но содержание его в поверхностном слое было выше, чем в нижележащих слоях (рис. 9). Наблюдения в природной обстановке подтвердили результаты лабораторных опытов, а также показали миграцию кальция в глубинные слои. Так, кальций проникает через 40 дней на глубину 12 см, а через 109 дней — на 22 см, причем наблюдается накопление его в более глубоких слоях (рис. 10).[. ]
Как видно из приведенных в табл. 7 данных, при 30-минутной обработке количества вытесненного кальция, определенные по нейтрализации НС1 и по радиоактивности, совпадают. При увеличении времени обработки соотношение между содержанием кальция в растворе и в поглощенном состоянии не изменялось, количество же нейтрализованной кислоты возрастало.[. ]
В настоящем сообщении описаны результаты проведенных авторами исследований с применением радиоактивного изотопа кальция для изучения обменных реакций в почвах и разработки на этой основе новой методики определения емкости поглощения почв, а также решения некоторых других методических вопросов.[. ]
С точки зрения угрозы населению для специалиста-гигиениста представляет интерес не только радиоактивное излучение как таковое и его интенсивность, но особенно характер излучения (ос-, Р- или у-излучение), предполагаемая его продолжительность (период полураспада) и особенно химическая природа носителей радиации (радионуклидов). Благодаря своим химическим свойствам отдельные радионуклиды значительно отличаются друг от друга по определяющей их биологическое воздействие продолжительности пребывания и месту накопления в организме и окружающей его среде (продуктах питания). Особенно опасен в этом отношении источник р-излучения 908г с периодом полураспада 28 лет, который вследствие своего химического сродства с кальцием откладывается в костях и надолго удерживается там. Некоторые радионуклиды, например 1311, быстро поглощаются скотом и через короткое время обнаруживаются в молоке; у человека они накапливаются в щитовидной железе.[. ]
Наши представления о геологических процессах в связи с этим коренным образом перестраиваются. Радиоактивный распад — все указывает — не ограничивается теми радиоактивными атомами, для которых это точно установлено: ураном, торием, калием, рубидием, самарием [6]. Они в зоны веков, непрерывно выделяя тепловую атомную энергию (излучение а, ?, 7), сами исчезают и создают атомы гелия, свинца, кальция, стронция (§ 91 )19.[. ]
Другой необходимый растениям двухвалентный катион— магний — может угнетать их, если в растворе нет кальция. Последний не способен к передвижению внутри растения сверху вниз (это доказано с помощью радиоактивного изотопа Ca46),? Отсюда важность нахождения кальция во всей зоне распространения когрней.[. ]
Удержанию радионуклидов в грунте способствует наличие в нем элементов, близких по химическим свойствам к радиоактивным изотопам. Например, кальций - элемент, близкий по свойствам к 90Бг, поэтому добавка к кислым почвам извести ведет к увеличению их поглотительной способности по отношению к этому изотопу. Калий и натрий похожи по своим свойствам на радиоактивный цезий (137Сз). Железо по некоторым свойствам, и особенно гидролизу, напоминает церий (144Се).[. ]
Начиная с 1987 года, загрязнение уже происходило через корневые системы растений. Говоря о корневом поступлении радиоактивных загрязнений, следует отметить, что в цезиевый период корневое поступление загрязнений определяют стронций-90 и цезий-137. Являясь химическими аналогами, соответственно, кальция и калия, они отличаются высокой биологической подвижностью. Причем, при внекорневом пути поступления наиболее подвижен цезий-137. Внекорневое поступление же стронция-90 происходит в десятки раз медленнее. И наоборот, при корневом пути поступления более подвижен стронций-90, который из почвы через корни легче поступает в растения.[. ]
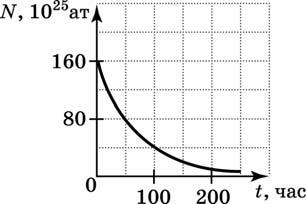
Каждому химическому элементу соответствуют разные типы атомов, все они имеют несколько различное строение, некоторые из них радиоактивны, другие — нет. Эти варианты элементов называются изотопами. Например, существует несколько изотопов кислорода, несколько изотопов углерода и т. д. Радиоактивные изотопы нестабильны и при распаде превращаются в другие изотопы, испуская при этом излучение. Каждый радиоактивный изотоп характеризуется определенным числом— атомным весом и распадается с определенной скоростью. Эту скорость принято называть периодом полураспада. Некоторые радиоактивные изотопы, имеющие важное значение для экологии, перечислены в табл. 59. Можно видеть, что 45Са — это радиоактивный изотоп кальция; его атомный вес равен 45 и каждые 160 дней он теряет половину своей радиоактивности. Период полураспада — величина, постоянная для данного изотопа (т. е. внешние факторы не влияют на скорость разрушения); для разных радиоактивных изотопов величина его варьирует от нескольких секунд до многих лет. В общем крайне «короткожи-вущие» радионуклиды не представляют интереса для экологии.[. ]
Кроме урана, тория и продуктов их распада в природе найдены следующие радионуклиды: калий — 40 (период полураспада — 4,5 ¦ 108 лет), кальций-48 (2 • 1016 лет), рубидий-87 (6,2 ¦ Ю10 лет), цирконий-96 (6,2 • 1016 лет), индий-115 (6,0 ¦ 1014 лет), олово-124 (1,5 • 1017 лет), сурьма-123 (1,0 • 10м лет), лантан-138 (7,0 • Ю10 лет), цезий-142 (1,0- 1015 лет), вольфрам-180 (2,2- 1017 лет), висмут-209 (2,7 ¦ 1017 лет). Среднее содержание естественных радиоактивных элементов в земной коре составляет около 0,1 % по весу.[. ]
Стронций — хороший пример ранее почти не изученного элемента, который сейчас служит объектом особого внимания, в связи с тем что радиоактивный стронций крайне опасен для человека и других позвоночных. По химическим свойствам стронций похож на кальций и поэтому, попав в организм, накапливается в костях и оказывается в тесном контакте с кроветворными тканями. Примерно 7% всего осадочного материала, стекающего вниз по рекам, составляет кальций. На каждые 1000 атомов кальция, движущихся к морю, приходится 2,4 атома стронция. Когда при производстве и испытаниях ядерного оружия, а также при работе атомных электростанций расщепляется уран, среди отходов оказывается радиоактивный стронций-90 — один из продуктов расщепления, характеризующийся очень длительным периодом полураспада.[. ]
Для уточнения времени взаимодействия по4 этому методу навески почвы (чернозем), насыщ тывались различное время 0,05 н. НС1. К соля меченый кальций. При обработке почвы 0,05 н. поглощенного кальция не достигается. Мы подбф которых вытеснялось около 90% поглощенного ответствующую поправку. Количество вытеснен валось по нейтрализации соляной кислоты. Эти разной продолжительности взаимодействия поч з всего кальция до 96,6%. Количество вытеененно рассчитано по радиоактивности (исходя из то кальций равномерно распределяется между ка растворе, и оставшимся в поглощенном состоя всех случаях вытеснялось примерно 90%, а 10 ном состоянии.[. ]
К опасным факторам антропогенного характера, способствующим серьезному ухудшению качества атмосферы, следует отнести ее загрязнение радиоактивной пылью. Так, при ядерных взрывах или авариях на АЭС большая часть радионуклидов образуется в результате деления урана-235, урана-238 и плутония-239. Установлено, что через несколько десятков секунд после взрыва образуются примерно 100 различных радионуклидов, 29 из которых вносят наибольший вклад в радиоактивное загрязнение атмосферы через час, 20 - через двое суток, а 3 - через 100 лет. Особую потенциальную опасность для человека и животных представляет стронций-90 не только как долгоживущий элемент, но и как аналог кальция, способный заменять его в костях. Во время ядерных взрывов радионуклиды находятся в газообразном состоянии и по мере понижения температуры конденсируются в аэрозольное облако. Наиболее крупные частицы (диаметром более 40 мкм) выпадают из атмосферы и оседают на земной поверхности. Мелкие же частицы (диаметром от 1 до 20 мкм) попадают не только в верхние слои тропосферы, но и в стратосферу, обусловливая так называемое глобальное загрязнение, сопровождающееся выпадением радионуклидов в пределах обоих полушарий.[. ]
Стронций-90, поступающий в биосферу, — новое вещество; он не существовал в природе до того, как человек расщепил атом. Ничтожные количества радиоактивного стронция, содержащиеся в осадках, выпадающих после испытаний атомного оружия, и утекающие из ядерных реакторов, мигрируют вместе с кальцием из почвы и воды в растения, животных и пищу человека, накапливаясь в его костях. По мнению некоторых медиков, в 1970 г. в костях людей содержалось уже достаточное количество стронция, чтобы он оказывал канцерогенное воздействие. Когда был объявлен международный запрет на испытание ядерного оружия в атмосфере, опасность на время уменьшилась. Радиоактивный цезий-137 — другой опасный продукт деления ядра по свойствам схож с калием и потому быстро циркулирует по пищевым цепям. Сейчас в резервуарах на атомных электростанциях хранятся большие количества радиоактивных продуктов расщепления. Как уже отмечалось, неумение избавляться от этих отходов мешает более широкому мирному использованию атомной энергии. Проблемы, связанные с опасными отходами, будут подробнее рассмотрены в гл. 5.[. ]
Наибольшую опасность в этом отношении представляют изотопы стронция (905г) и цезия (137Сб), поскольку именно они обусловливают искусственную радиоактивность, характеризуются длительным периодом полураспада (28 лет у 905г и 33 года у 137Сз), обладают высокой энергией излучения и способностью активно включаться в биологический круговорот. Поэтому чрезвычайно важно знать закономерности, связанные с поглощением этих изотопов почвами, их миграцией и поступлением в растения. Общим для "Эг и 137Сэ является довольно полное их поглощение твердой фазой почвы, поэтому основное их количество (80—90 %) закрепляется в самом верхнем слое (5—9 см). При этом наибольшей сорбцией обладают почвы с высоким содержанием гумуса, богатые илистой фракцией и с монтмориллонитовым и гидрослюдистым составом глинистых минералов. По своим свойствам "Эг близок к кальцию, а 137Сз— к калию. Поэтому поведение этих радиоизотопов близко к поведению указанных химических элементов.[. ]
Выделение стронция-9 0. В 10 л пробы вносят по 50 мг/л (в пересчете на металл) нитратных растворов носителей стронция, бария, лантана и церия и добавляют раствор хлорида кальция 20 мг/л (по кальцию). Перемешивают, нагревают до 80° С, прибавляют 10%-ный раствор карбоната натрия из расчета 580 мг/л для осаждения карбоната кальция. Воду с осадком отстаивают 2—3 ч, сливают, осадок растворяют в нескольких миллилитрах концентрированной азотной кислоты и разбавляют дистиллированной водой до объема 50—100 мл. Раствор переносят в стакан вместимостью 200—300 мл, добавляют 10 мл 0,5%-ного раствора хлорида железа (III), нагревают до кипения и осаждают гидроксид железа (III) аммиаком, не содержащим С02. Осадок отделяют, промывают 2—3 раза слабым раствором аммиака и отбрасывают. Раствор и промывные воды нейтрализуют 6 н. раствором азотной кислоты, прибавляют 1 мл 6 н. раствора уксусной кислоты, 2 мл 6 н. раствора ацетата аммония, нагревают до 70—80° С и добавляют 1—2 мл 1,5 н. раствора хромата натрия. После осаждения хромата бария осадок отделяют, промывают разбавленным раствором ацетата аммония и отбрасывают. К оставшемуся раствору прибавляют хлорид железа (III) и повторяют осаждение гидроксида железа. После этого добавляют аммиак до пожелтения раствора и насыщенный раствор карбоната аммония до полноты осаждения карбоната стронция. Выпавший осадок отстаивают 2—3 ч, проверяют полноту осаждения, центрифугируют, промывают водой, растворяют в концентрированной азотной кислоте и разбавляют дистиллированной водой до объема 50 мл. Затем замеряют объем азотнокислого раствора н отбирают 1 мл для определения химического выхода носителя стронция. После этого вносят 50 мг в пересчете на металл раствора носителя иттрия и оставляют на 6 дней для 75%-ного накопления иттрия-90. Затем осаждают свободным от углекислоты аммиаком гидроксид иттрия и отмечают время отделения иттрия-90 от стронция-90. Осадок гидроксида иттрия 2—3 раза промывают слабым раствором аммиака, подсушивают на фильтре и во взвешенном тигле прокаливают при 900° С. Осадок взвешивают, наносят на мишень и на малофоновой установке измеряют радиоактивность.[. ]
При изучении химического состава вод определяют содержание минеральных, газовых и органических компонентов. Среди минеральных компонентов, как правило, анализируют содержание кальция, магния, натрия, калия, хлор-, сульфат-, карбонат- и бикарбонат-ионов и некоторых микрокомпонентов — стронция, бария, иода, брома, бора, азота, иногда лития и радиоактивных элементов. При этом используют обычные комплексонометриче-ские (трилонометрические) методы, пламенную фотометрию, а также классические титриметрические и гравиметрические методы анализа. Содержание основной массы неорганических веществ в подземных водах измеряется десятками и сотнями граммов, микрокомпонентов — десятками и сотнями миллиграммов на литр исследуемой воды.[. ]
РАДИОАКТЙВНОСТЬ [лат. radiare излучать, испускать лучи + activus деятельный] — самопроизвольное выделение энергии в виде потока частиц (альфа- и бета-частицы) и квантов электромагнитной энергии (гамма-излучение) радиоактивными изотопами (радионуклидами). Имеются четыре естественных радиоактивных семейства: урана, актиния, тория и плутония. Природные радиоактивна элементы, не входящие в состав радиоактивных семейств: углерод, рубидий, олово, самарий, лютеций и продукты их распада (азот, кальций, аргон, стронций и др.). Существует около 1700 искусственных радионуклидов. Р. наведенная (радиация наведенная) — Р. вызванная потоком нейтронов. При ядерном взрыве нейтроны, достигающие поверхности земли, взаимодействуют с ядрами атомов, входящих в состав грунта, разной техники, сооружений и других объектов. В результате поглощения нейтронов ядрами устойчивых элементов последние превращаются в радиоактивные изотопы. Большинство их сравнительно быстро распадается, превращаясь в устойчивые нерадиоактивные элементы. Степень Р. и. зависит от мощности и вида атомного взрыва, состава почвы и расстояния до центра взрыва.[. ]
В 1934 г. касаясь этого вопроса в «Очерках геохимии», я пришел к заключениям, которые остаются неизменными и сейчас [23]. Рассеяние иода полное, напоминает в некотором отношении сделавшееся нам привычным нахождение радиоактивных элементов. Иод является по характеру своего нахождения как бы моделью радия. Его можно найти во всех без исключения минералах, в которых он собирается в различных, иногда относительно значительных количествах. Многочисленные измерения Фелленберга и других [24] дают пределы от 3,8 • 10“л (борнит) до 5 • 10”Е)% по весу (кальцит), причем химически это нельзя объяснить.[. ]
Появление метода меченых атомов открыло новые возможности дальнейшего изучения обменных реакций в почвах и разрешения ряда методических вопросов. Среди элементов, принимающих участие в обменных процессах в почвах, важнейшее значение принадлежит кальцию. Для изучения обменных реакций с участием иона кальция может быть использован радиоактивный изотоп кальция — Са45.[. ]
Некоторые из элементов с нечетным атомным номером, такие, как, например, Р, Мп, А1, в природе вообще представлены только одним стабильным изотопом. Для получения меченых соединений большинства биологически важных элементов используют возможность получения их искусственных радиоактивных изотопов. В агрохимических исследованиях используются радиоактивные изотопы фосфора (Р32), серы (Б35), углерода (С14), кальция (Са45), железа (Ее59), водорода (Н3 или Т) и некоторые другие радиоактивные изотопы.[. ]
На длительно эксплуатируемых месторождениях увеличение обводненности и особенно - использование слабоминерализованной воды для поддержания пластового давления приводит к выщелачиванию из горных пород все возрастающих количеств радионуклидов. Как следствие они, осаждаясь с солями бария, кальция и стронция, образую! радиоактивные отложения, удельная активность которых иногда в сотни раз превышает средние значения природного характера.[. ]
Применение изотопных методов исследования, позволяющих осуществлять наблюдения за распределением в растении питательного вещества, поступившего в течение определенного периода времени, представляет поэтому большой интерес для изучения минерального питания плодовых растений. В настоящем сообщении описаны результаты исследований, проведенных нами с применением радиоактивных изотопов для изучения поступления фосфора и кальция в яблоню во время цветения и распускания почек.[. ]
Большое значение ионный обмен имеет в агрохимии, процессах жизнедеятельности и химическом анализе. Метод ионообменной сорбции применяют для умягчения или обессоливания воды (например, для опреснения морской воды), удаления солей из сахарных сиропов, молока, вин, растворов фруктозы, дубильных веществ, продуктов гидролиза сельскохозяйственного сырья, растворов лекарственных препаратов (антибиотиков, витаминов, алкалоидов), для удаления ионов кальция из плазмы крови перед ее консервацией, для очистки от минеральных ионов растворов органических реагентов, для очистки сточных вод от фенола и тяжелых металлов, а также для извлечения (концентрирования) ценных ионов, находящихся в микродозах в растворе (например, редкоземельных элементов). Ионный обмен широко применяют в гидрометаллургии — для извлечения благородных, цветных и редких металлов из сбросных растворов (например, ионов из стоков гальванических цехов), для улавливания и концентрирования радиоактивных ионов и ионов меди из стоков медноаммиачного производства искусственного шелка [4].[. ]
Грибам, обволакивающим корни растения-хозяина, в качестве источника углерода необходимы растворимые углеводы, и в этом отношении они отличаются от большинства своих сво-бодноживущих, т. е. несимбиотических родичей, расщепляющих целлюлозу. Микоризные грибы то крайней мере часть своих потребностей в углероде удовлетворяют за счет хозяев. Мицелий всасывает из почвы минеральные биогены, и